16/02/18
Sciences et technologie
Des chercheurs strasbourgeois du laboratoire Modèles insectes d’immunité innée (CNRS) et de l’Institut pluridisciplinaire Hubert-Curien (CNRS / Université de Strasbourg) ont mis en évidence un mécanisme original de reconnaissance des infections chez la mouche drosophile. Il permet de détecter l’activité des enzymes microbiennes responsables de la virulence, plutôt que des motifs moléculaires spécifiques des microorganismes, qui constituent des signaux de « non-soi ». Ces résultats ont été publiés le 15 février 2018 dans la revue Molecular Cell.
L’immunité innée, commune à tous les organismes vivants, est la première barrière contre les infections. Pour se défendre, la reconnaissance des pathogènes est une question cruciale qui se pose pour tous les organismes. Dès les années 80, le professeur Jules Hoffmann, ancien directeur du laboratoire Modèles insectes d’immunité innée, et ses collaborateurs se sont intéressés aux mécanismes d’immunité innée des insectes et, en particulier celui de la drosophile, un modèle de recherche puissant car dépourvu de réponse immunitaire adaptative.
Au cours des années 90, leurs travaux ont conduit à la découverte du récepteur Toll. Ils ont montré que, lors d'infections par des bactéries ou des champignons, ce récepteur contrôle la réponse immunitaire et la production de peptides anti-microbiens chez la drosophile. Lors d’une infection, le récepteur Toll peut être activé de deux manières, soit par la détection de sucres spécifiquement présents à la surface des microbes ; soit par la détection d'enzymes, appelées protéases, sécrétées par un nombre important de pathogènes. Cette seconde voie d’activation comporte encore de nombreuses zones d’ombres.
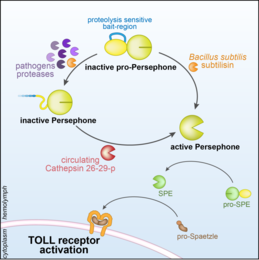
Dans les résultats qui viennent de paraître, Florian Veillard, Jean-Marc Reichhart et leurs collaborateurs identifient le mécanisme moléculaire qui permet la détection des microbes pathogènes chez la mouche drosophile. Ils ont montré pour la première fois comment un récepteur de l’immunité innée, Perséphone, peut être activé par un signal de danger, en l’occurrence les activités enzymatiques microbiennes responsables de la virulence. Le mécanisme décrit permet une détection plus spécifique/fine des infections que la détection de motifs moléculaires comme des sucres, qui peuvent être présents dans la flore microbienne hébergée par les animaux.
Ces résultats pourraient aboutir à l'identification de mécanismes apparentés chez les mammifères. De tels mécanismes, s’ils existent, pourraient expliquer en partie comment le système immunitaire humain est capable de faire la différence entre les bactéries et champignons pathogènes et les microorganismes ne représentant pas de danger tels que ceux constituant la flore microbienne.
Document(s) à télécharger
- Nom du fichier : CP_Persephone_Molecular_c… Poids du fichier : 261 Ko